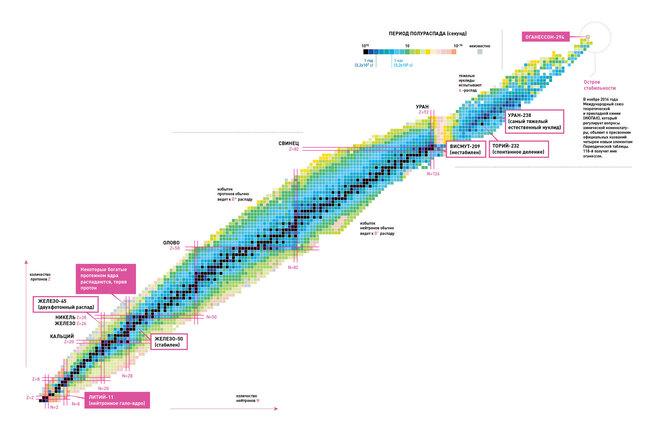
Kufijtë e tabelës periodike të elementeve. Ku është ishulli i lumtur i stabilitetit?
A ka tabela periodike e elementeve një kufi "të sipërm" - pra, a ka një numër atomik teorik për një element super të rëndë që do të ishte e pamundur të arrihet në botën e njohur fizike? Fizikani rus Yuri Oganesyan, pas të cilit është emëruar elementi 118, beson se një kufi i tillë duhet të ekzistojë.
Sipas Oganesyan, kreu i laboratorit Flerov në Institutin e Përbashkët për Kërkime Bërthamore (JINR) në Dubna, Rusi, ekzistenca e një kufiri të tillë është rezultat i efekteve relativiste. Ndërsa numri atomik rritet, ngarkesa pozitive e bërthamës rritet, dhe kjo, nga ana tjetër, rrit shpejtësinë e elektroneve rreth bërthamës, duke iu afruar kufirit të shpejtësisë së dritës, shpjegon fizikani në një intervistë të botuar në numrin e prillit të revistës. . Shkencëtar i ri. “Për shembull, elektronet më afër bërthamës në elementin 112 udhëtojnë me 7/10 shpejtësia e dritës. Nëse elektronet e jashtme do t'i afroheshin shpejtësisë së dritës, kjo do të ndryshonte vetitë e atomit, duke shkelur parimet e tabelës periodike”, thotë ai.
Krijimi i elementeve të rinj tepër të rëndë në laboratorët e fizikës është një detyrë e lodhshme. Shkencëtarët duhet, me saktësinë më të madhe, të balancojnë forcat e tërheqjes dhe zmbrapsjes midis grimcave elementare. Ajo që nevojitet është një numër "magjik" i protoneve dhe neutroneve që "ngjiten së bashku" në bërthamë me numrin e dëshiruar atomik. Vetë procesi i përshpejton grimcat në një të dhjetën e shpejtësisë së dritës. Ekziston një shans i vogël, por jo zero, për formimin e një bërthame atomike super të rëndë të numrit të kërkuar. Atëherë detyra e fizikantëve është ta ftohin atë sa më shpejt që të jetë e mundur dhe ta "kapin" në detektor para se të prishet. Sidoqoftë, për këtë është e nevojshme të merren "lëndët e para" të përshtatshme - izotopë të rrallë, jashtëzakonisht të shtrenjtë të elementeve me burimet e nevojshme neutron.
Në thelb, sa më i rëndë të jetë një element në grupin e transaktinideve, aq më e shkurtër është jeta e tij. Elementi me numër atomik 112 ka një gjysmë jetëgjatësi prej 29 sekondash, 116 - 60 milisekonda, 118 - 0,9 milisekonda. Besohet se shkenca arrin kufijtë e materies fizikisht të mundshme.
Megjithatë, Oganesyan nuk është dakord. Ai paraqet këndvështrimin se është në botën e elementëve super të rëndë. "Ishulli i Stabilitetit". "Koha e zbërthimit të elementeve të rinj është jashtëzakonisht e shkurtër, por nëse shtoni neutrone në bërthamat e tyre, jetëgjatësia e tyre do të rritet," vëren ajo. “Shtimi i tetë neutroneve në elementët e numëruar 110, 111, 112 dhe madje 113 zgjat jetën e tyre me 100 vjet. një herë".
Emërtuar sipas Oganesyan, element Oganesson i përket grupit të transaktinideve dhe ka numrin atomik 118. Ai u sintetizua për herë të parë në vitin 2002 nga një grup shkencëtarësh rusë dhe amerikanë nga Instituti i Përbashkët për Kërkime Bërthamore në Dubna. Në dhjetor 2015, ai u njoh si një nga katër elementët e rinj nga Grupi i Përbashkët i Punës IUPAC/IUPAP (një grup i krijuar nga Unioni Ndërkombëtar i Kimisë së Pastër dhe të Aplikuar dhe Unioni Ndërkombëtar i Fizikës së Pastër dhe të Aplikuar). Emërtimi zyrtar u bë më 28 nëntor 2016. Oganesson ma numri më i lartë atomik i masa më e madhe atomike ndër të gjithë elementët e njohur. Në 2002-2005, u zbuluan vetëm katër atome të izotopit 294.
Ky element i përket grupit të 18-të të tabelës periodike, d.m.th. gaze fisnike (duke qenë përfaqësuesi i tij i parë artificial), megjithatë, ai mund të tregojë reaktivitet të konsiderueshëm, ndryshe nga të gjithë gazrat e tjerë fisnikë. Në të kaluarën, oganesson mendohej të ishte një gaz në kushte standarde, por parashikimet aktuale tregojnë për një gjendje konstante grumbullimi në këto kushte për shkak të efekteve relativiste që Oganessian përmendi në intervistën e cituar më parë. Në tabelën periodike, është në bllokun p, duke qenë rrënja e fundit e periudhës së shtatë.
Studiuesit rusë dhe amerikanë kanë propozuar historikisht emra të ndryshëm për të. Në fund, megjithatë, IUPAC vendosi të nderojë kujtimin e Hovhannisyan duke njohur kontributin e tij të madh në zbulimin e elementëve më të rëndë në tabelën periodike. Ky element është një nga dy (pranë bregut të detit) me emrin e një personi të gjallë.

